Descoperire: lizozomii din tumori pot reține medicamentele PARP și creează distribuţii inegale în tratamentul cancerului
Cercetătorii arată că lizozomii din celulele tumorale pot reține inhibitorii PARP, creând depozite care provoacă o distribuţie inegală a medicamentului și influențează eficacitatea tratamentului.
Sursa foto: Sciencedaily
O revelație în felul în care medicamentele împotriva cancerului se distribuie în tumori
O echipă de cercetare de la MRC Laboratory of Medical Sciences (LMS) a identificat un mecanism ascuns care explică parțial de ce aceleași tratamente împotriva cancerului funcționează extrem de bine la unii pacienți și eșuează la alții. Studiul, publicat în Nature Communications și condus de Dr. Louise Fets, a urmărit comportamentul inhibitorilor PARP în mostre de tumori ovariene umane folosind tehnici avansate de imagistică moleculară.
Imaginea detaliată a unei distribuţii inegale
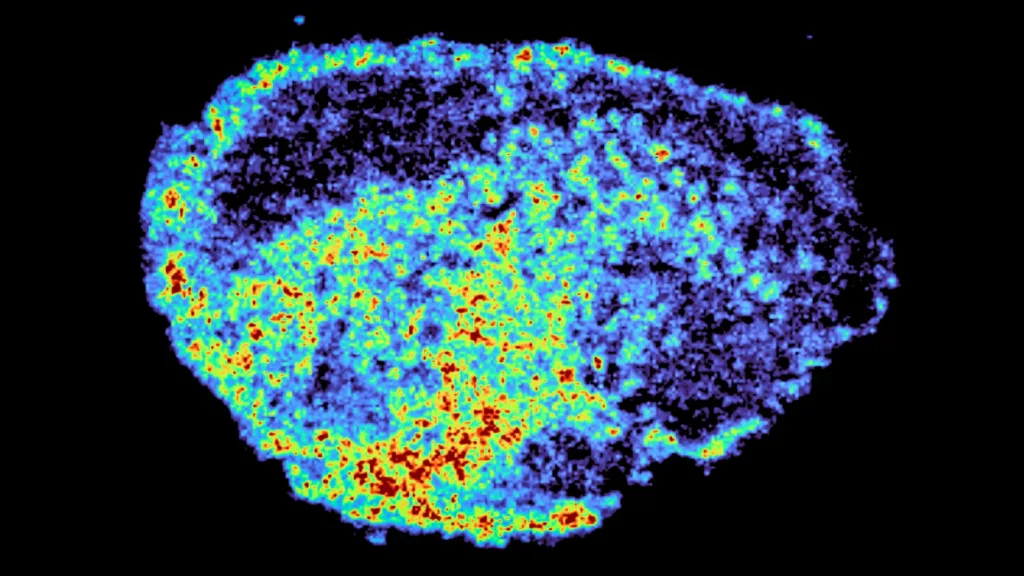
Cercetătorii au utilizat felii subțiri din tumori ovariene recoltate de la pacienți și menținute viabile în laborator — așa-numitele „explante” — pentru a urmări modul în care medicamentele pătrund și se distribuie în țesut tumoral real. Folosind imagistică prin spectrometrie de masă, echipa a generat hărți detaliate ale localizării moleculelor de medicament în interiorul probelor. Aceste hărți au arătat regiuni cu acumulări mari, denumite „hotspoturi”, și zone cu niveluri reduse ale medicamentului, evidențiind disparităţi marcante atât în cadrul aceleiași tumori, cât şi între pacienți care au primit aceeași doză.
Imaginea oferită de echipă ilustrează inhibitorul PARP niraparib în țesut tumoral ovarian uman; culorile calde indică regiuni cu acumulare mare a medicamentului, iar culorile reci indică regiuni cu niveluri scăzute.
Combinarea hărților moleculare cu activitatea genetică
Pe lângă măsurarea distribuţiei medicamentului, cercetătorii au integrat date de spatial transcriptomics pentru a determina ce gene erau active în regiunile cu acumulare mare comparativ cu cele cu acumulare mică, toate din aceeași felie de țesut. Această abordare multimodală a permis investigarea relației dintre localizarea medicamentului și semnătura moleculară a celulelor din aceleași zone, oferind o perspectivă asupra motivelor care stau la baza variației observate.
Dr. Zoe Hall, autoare senioră și conferențiară asociată la Imperial College London, a subliniat importanța metodei: traducerea vizuală a moleculelor de medicament în țesutul pacientului a oferit posibilitatea de a compara, pe aceeași secțiune, zonele cu acumulare mare și mică și expresia genică asociată.
Lizozomii: rezervoare ascunse care modelează expunerea celulară
O descoperire centrală a studiului este rolul lizozomilor — organele celulare implicate în reciclarea componentelor celulare — în captarea anumitor inhibitori PARP. Anumiți agenți terapeutici sunt atrași în interiorul lizozomilor și rămân acolo, creând depozite intracelulare care eliberează treptat medicamentul. Acest fenomen transformă lizozomii în rezervoare cu eliberare lentă, ceea ce poate duce la expuneri foarte diferite între celule adiacente: unele celule stau sub o concentrație ridicată a medicamentului pentru perioade prelungite, în timp ce altele rămân practic neafectate.
Echipa a observat o variabilitate considerabilă la nivelul unei singure celule în ceea ce privește acumularea medicamentului: această variabilitate a fost determinată, în mare parte, de stocarea medicamentului în lizozomi. Dr. Carmen Ramirez Moncayo, autoare principală și cercetător postdoctoral la LMS, a remarcat surprinderea echipei în fața acestei diferențe mari între celule și a explicat că lizozomii acționează ca rezervoare care cresc expunerea unor celule la medicament, prin depozitarea și eliberarea ulterioară a acestuia.
Nu toți inhibitorii PARP se comportă la fel
Studiul a arătat că nu toți inhibitorii PARP sunt afectați în același mod de fenomenul de acumulare lizozomală. Analiza a indicat că medicamente precum rucaparib și niraparib sunt susceptibile de a fi capturate și stocate în lizozomi, în timp ce altele, precum olaparib, par să nu fie influențate de acest mecanism. Această diferență între compuși sugerează că proprietățile chimice ale fiecărui inhibitor influențează probabil tendința de a se localiza în lizozomi și, implicit, modul în care se distribuie în interiorul tumorii.
- Rucaparib și niraparib prezintă acumulare în lizozomi
- Olaparib nu este afectat în mod similar
Implicații pentru tratamente personalizate și rezistență
Inhibitorii PARP au transformat tratamentul pentru anumite cancere, în special pentru cancerul ovarian, și sunt utilizați și în forme de cancer de sân sau de prostată, fiind testați în multe alte tipuri de tumori. Descoperirea că lizozomii pot crea depozite de medicament și, prin aceasta, o distribuție heterogenă la nivel celular, are implicații practice importante. În primul rând, eficacitatea unui tratament nu depinde doar de capacitatea medicamentului de a ajunge la tumoare, ci și de modul în care acesta se împarte în interiorul tumorii și al celulelor sale.
Înțelegerea acestor mecanisme ar putea conduce la strategii terapeutice mai bine adaptate la particularitățile fiecărei tumori: evaluarea semnăturii moleculare a tumorii unui pacient ar putea ajuta la alegerea inhibitorului PARP cel mai potrivit sau la combinarea tratamentelor astfel încât depozitarea lizozomală să nu compromită eficiența generală.
Dr. Louise Fets, autoare senioră și șefa grupului Drug Transport and Tumour Metabolism la LMS, a explicat speranța echipei: prin studierea modului în care medicamentele sunt absorbite în celule, cercetătorii pot înțelege influența acestor procese asupra faptului că terapiile funcționează pentru unii pacienți și nu pentru alții și, în viitor, pot folosi semnătura moleculară a tumorii pentru a personaliza mai bine abordările terapeutice.
Limitările studiului și pașii următori
Autorii subliniază că experimentul a fost realizat pe țesut tumoral menținut ex vivo, iar în context clinic medicamentele sunt administrate prin fluxul sanguin. În organism, vasele tumorale sunt adesea deformate și dezorganizate, ceea ce poate agrava distribuţia inegală a medicamentului. Din acest motiv, cercetătorii intenționează să extindă studiile folosind modele animale și grupuri mai mari de pacienți pentru a înțelege mai bine interacțiunea dintre modul de administrare, structura tumorală și stocarea lizozomală în condiții clinice, inclusiv în cancere recidivate.
Finanțare și recunoaștere
Studiul a fost susținut financiar de mai multe organizații: Medical Research Council, Cancer Research UK, o bursă doctorală din partea Integrative Toxicology Training Partnership administrată de MRC Toxicology Unit și un premiu Victoria’s Secret Global Fund for Women’s Cancers Career Development Award, acordat în parteneriat cu Pelotonia și AACR. Așa cum se menționează în materialele echipei de cercetare, aceste finanțări au sprijinit resursele necesare pentru abordarea multimodală și analiza detaliată a probelor umane.
Referință științifică
Lucrarea completă, care detaliază metodele și rezultatele experimentale, este publicată în Nature Communications sub titlul: „Multimodal imaging reveals a lysosomal drug reservoir that drives heterogeneous distribution of PARP inhibitors.” DOI-ul publicat este http://dx.doi.org/10.1038/s41467-026-70558-1.
Autorii lucării includ: Carmen R. Moncayo, Restuadi Restuadi, Guanying Zhang, Daniel Marks, Paula Ortega-Prieto, Emily Doherty, Nathalie Lambie, Chad Whilding, Ivan Andrew, Alex Montoya, Bhavik Patel, Katie Tyson, Betheney R. Pennycook, Lauren Pendergast, Vincen Wu, Zoltan Takats, Nik Matthews, George R. Young, Priyanka Verma, Pavel Shliaha, Laurence Game, Boris Lenhard, Iain McNeish, Christina Fotopoulou, Alexis R. Barr, Paula Cunnea, Zoe Hall și Louise Fets.
Pentru lectură suplimentară și context editorial al comunicatului, materialul sintetic al studiului este disponibil public pe pagina instituțională a prezentării: https://www.sciencedaily.com/releases/2026/03/260326075550.htm.
Descoperirea evidențiază cât de mult detaliile la scară celulară pot influența rezultatele clinice și subliniază necesitatea unor metode care să cartografieze distribuţia medicamentelor în țesutul tumoral pentru a ghida terapiile viitoare.







